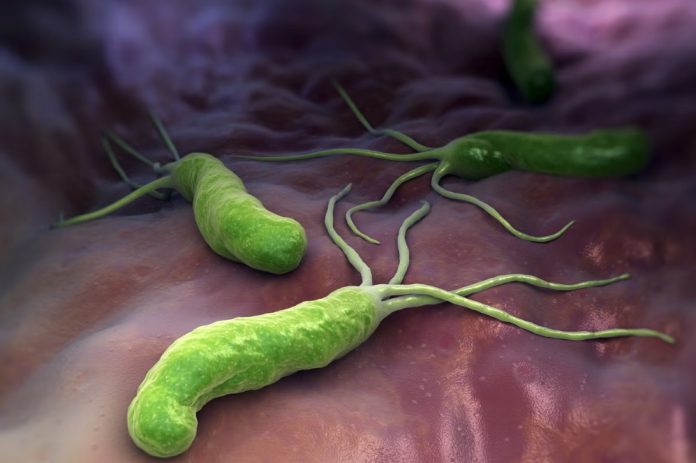
ในขณะที่นักวิทยาศาสตร์ทั่วโลกยังคงพยายามค้นหาทางรักษาโรคอัลไซเมอร์(Alzheimer’s disease) เพื่อไม่ให้ทุกๆ 3 วินาที จะมีคนหนึ่งบนโลกถูกวินิจฉัยว่าเป็นโรคสมองเสื่อม การค้นพบครั้งใหม่กลับมาจากแหล่งที่ไม่คาดคิด แบคทีเรียที่เป็นต้นเหตุของแผลในกระเพาะอาหาร อาจถือกุญแจสำคัญในการหยุดยั้งการสะสมของโปรตีนพิษที่เกี่ยวข้องกับอัลไซเมอร์ได้
งานวิจัยซึ่งตีพิมพ์โดยทีมของนักวิทยาศาสตร์พบว่า Helicobacter pylori แบคทีเรียที่มักเป็นสาเหตุของแผลในกระเพาะอาหาร โปรตีนส่วนหนึ่งของแบคทีเรียชนิดนี้ที่มีชื่อว่า CagANสามารถยับยั้งการรวมตัวของโปรตีน อะไมลอยด์-เบตา และ เทา ซึ่งเป็นสองโปรตีนหลักที่ทำให้สมองเสื่อมตามแบบที่พบในโรคอัลไซเมอร์ได้ ซึ่งโปรตีนอะไมลอยด์-เบตาจะก่อตัวเป็นคราบเหนียวเกาะรอบเซลล์สมอง ขณะที่โปรตีนเทาจะบิดเกลียวรวมกันภายในเซลล์ นำไปสู่การตายของเซลล์ประสาทในระยะยาว
นอกจากนี้ CagAN ยังสามารถยับยั้งการรวมตัวของโปรตีนที่เกี่ยวข้องกับโรคพาร์กินสันและเบาหวานชนิดที่ 2 ได้ด้วย ซึ่งบ่งชี้ถึงความเป็นไปได้ในการพัฒนายาเพื่อรักษาหลายโรคที่เกี่ยวข้องกับโปรตีนผิดปกติ แม้จะยังเป็นเพียงการทดลองยังอยู่ในห้องปฏิบัติการ แต่ผลที่ได้บ่งชี้ถึงศักยภาพของแนวทางการรักษาแบบใหม่ที่อาจเปลี่ยนอนาคตของโรคที่เกี่ยวข้องกับโปรตีนผิดปกติในระดับโครงสร้าง งานวิจัยนี้ยังตั้งคำถามใหม่ต่อความเข้าใจเดิม ๆ เกี่ยวกับ H. pylori ซึ่งเคยถูกมองว่าเป็นเชื้ออันตรายอย่างสิ้นเชิงว่า ในอนาคตเราอาจต้องหันมาเข้าใจให้ลึกซึ้งมากขึ้นว่า อะไรคือส่วนที่เป็นภัย และอะไรที่อาจเป็นประโยชน์ต่อมนุษย์
While scientists around the world continue to search for a cure for Alzheimer’s disease—so that one more person isn’t diagnosed with dementia every three seconds—a surprising new discovery has emerged from an unexpected source. A bacterium known for causing stomach ulcers may hold the key to preventing the toxic protein buildup linked to Alzheimer’s.
A study published by a team of scientists found that Helicobacter pylori, a common cause of gastric ulcers, produces a protein fragment called CagAN that can effectively inhibit the aggregation of amyloid-beta and tau—the two main proteins responsible for the hallmark brain degeneration seen in Alzheimer’s disease. Typically, amyloid-beta forms sticky plaques around brain cells, while tau proteins twist into tangles inside cells, eventually leading to the death of neurons.
Remarkably, CagAN was also shown to block the aggregation of proteins associated with Parkinson’s disease and type 2 diabetes, suggesting a broader therapeutic potential for treating multiple diseases caused by abnormal protein buildup.
Although the research is still in the laboratory phase and has not yet been tested in animals or humans, the findings point toward a promising new approach that could reshape the future of treating Alzheimer’s and other protein-misfolding disorders. The study also challenges the long-standing view of H. pylori as purely harmful, suggesting that in the future, we may need a more nuanced understanding of microbes—distinguishing between what is dangerous and what might, surprisingly, be beneficial to human health.
#Alzheimers #BrainHealth #PreventDementia #updatenews #TheThailanders
ที่มา : www.sciencealert.com